
Физико химический анализ жидких систем и электрические свойства их компонентов
Работы Н. А. Трифонова в период его кратковременного пребывания на кафедре физической химии Ростовского университета по физико-химическому анализу жидких систем были продолжены его последователями.
С. П. Мискиджьян различными методами физико-химического анализа изучил систему уксусная кислота - азотная кислота. Судя по диаграмме плавкости, эти кислоты реагируют между собой и дают молекулярное соединение состава 1:1.
Образование такого соединения подтверждается резко выраженным максимумом на изотермах вязкости. Но, поскольку система уксусная кислота - азотная кислота относится к иррациональным, по диаграмме вязкости нельзя судить о составе соединения. Косвенное указание на его образование дает изотерма показателя преломления, которая имеет явную выпуклость от оси составов.
Изотерма электропроводности, имея вогнутость к оси составов, тоже указывает на образование химического соединения, но оно не является в сколько-нибудь заметной степени электролитом.
Что касается изотерм плотности и поверхностного натяжения, то они близки к аддитивности и не подтверждают химического взаимодействия компонентов. Однако С. П. Мискиджьян считает, что при углублении анализа указанных изотерм они химически взаимодействуют.1
1 (С. П. Мискиджьян. Физико-химический анализ системы уксусная кислота - азотная кислота. Диссертация на соискание ученой степени кандидата химических наук. Ростов-на-Дону, 1945, стр. 103.)
С. П. Мискиджьян убедительно показал, что литературные даны Пиктэ относительно существования соединения уксусной кислоты с азотной состава 2:1 (2 молекулы уксусной кислоты), якобы перегоняющегося без разложения при 127°, несостоятельны. Образование и строение соединения состава 1:1 он истолковывает с точки зрения теории кислот и оснований Бренстеда и наглядно представляет схемой
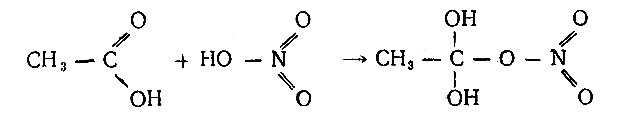
С. П. Мискиджьян успешно продолжает развивать работы по физико-химическому анализу жидких систем на кафедре биохимии Львовского медицинского института. Диссертацию на степень кандидата химических наук он защитил в Ростовском университете в 1945 г.
Энергично начал исследования по физико-химическому анализу жидких систем О. А. Осипов. Под руководством Н. А. Трифонова он завершил кандидатскую диссертацию "Поверхностное натяжение рациональных двойных жидких систем"1, которую успешно защитил в заседании Ученого совета университета 11 октября 1947 г.
1 (О. А. Осипов. Поверхностное натяжение рациональных двойных жидких систем. Диссертация на соискание ученой степени кандидата химических наук. Ростов-на-Дону, 1947.)
Исследования были предприняты для опытного обоснования десяти возможных типов изотерм поверхностного натяжения рациональных жидких систем, теоретически выведенных Н. А. Трифоновым. Кроме того, ставилась задача - получить экспериментальные данные по температурным коэффициентам поверхностного натяжения систем, компоненты которых дают химические соединения; это нужно было для вычисления полной поверхностной энергии.
Методом Кантора - Ребиндера в сосудике конструкций Н. А. Трифонова были измерены поверхностное натяжение двадцати одной двойной жидкой системы в широком интервале температур, что позволило ему дать подробную характеристику их по изотермам поверхностного натяжения и распределить согласно классам жидких систем Н. А. Трифонова. Была также экспериментально подтверждена реальность существования систем типов: четыре, пять и семь, ранее теоретически обоснованных Н. А. Трифоновым.
Показано, что жидкие системы, компоненты которых относятся к разным классам органических соединений, могут иметь одинаковые типы диаграмм поверхностного натяжения. Наоборот, системы с компонентами одного класса органических соединений могут резко отличаться по типу изотерм поверхностного натяжения. Обращает внимание интересный факт, установленный экспериментально, что и в случаях, когда компоненты системы химически не взаимодействуют, изотермы поверхностного натяжения могут быть выпукло-вогнутые. О. А. Осипов, вычислив по уравнению Гиббса-Гельмгольпа значения полной поверхностной энергии, показал независимость ее от температуры.
Однако более результативные в теоретическом отношении работы О. А. Осипов развернул в последующие годы, когда при изучении компонентов систем были использованы электрические, электрохимические и магнитные методы исследования.
Так, для выяснения комплекоообразующей способности элементов 4-й группы периодической системы Д. И. Менделеева с органическими аддендами изучены более 100 комплексных соединений титана, циркона, тория, кремния и германия; определены их дипольные моменты и поляризация, теплоты образования и теплоты смешения, электропроводность, магнитная восприимчивость, рефракция и другие свойства; выявлены электрические свойства внутрикомплексных соединений индия, хрома, меди, бериллия, кадмия, цинка, алюминия, тория, циркония в растворах и в твердой фазе.
В результате установлено, что в галогенидах типа МГ4, где М - титан, олово, цирконий, торий, имеющие незаконченный р- и d-электронные уровни, атомы, стремясь к их заполнению, проявляют акцепторные свойства. Это подтверждает наличие большого количества комплексов типа продуктов присоединения.
Галогениды титана, олова, циркония дают с азот- и кислородсодержащими органическими веществами комплексные соединения с высокой полярностью. Увеличение дипольного момента в комплексных соединениях указанного типа наблюдается по мере роста ковалентного радиуса центрального атома.
О. А. Осипов предлагает оценивать экранирование в молекулярных соединениях по отношению неличин ковалентных радиусов центрального элемента и галогена. Наиболее прочные соединения образуются в случаях, когда отношения ковалентных радиусов близки к величине октаэдрического радиуса центрального атома. Показано, что величина электроотрицательности центрального атома не играет существенной роли при комплексообразовании. Здесь доминируют стерические факторы и величины дисперсионного эффекта связи металл - галоген. Предложена пространственная конфигурация комплексных соединений с координационным числом шесть. Так, комплексы олова, титана и циркония имеют цис-строение, а тория - транс-конфигурацию. Установлено строение то-копроводящих комплексов и дана схема электролитической диссоциации.
О. А. Осипов показал, что в комплексных соединениях титана состава 1:1 органические адденды активированы более сильно, чем в соединении состава 1:2. Поэтому некоторые эфираты могут разлагаться с образованием хлористых алкилов и трихлортитанацетата. Для элементов 4-й группы эта реакция проведена впервые. Таким способом можно получить кислородорганические соединения титана и циркония. Склонность к указанному разложению тем больше, чем выше отрицательный индукционный эффект у кислотного радикала и чем меньше электроотрицательность спиртового радикала в молекуле сложного эфира.
Высказано предположение, что в случаях, когда в реакциях полимеризации требуется сокатализатор, активным началом полимеризации будет полярный комплекс из катализатора и сокатализатора. Он должен быть малопрочным, а это возможно, если электроотрицательность адденда будет высокая. Разработана схема каталитического действия четырех-хлористого титана и сокатализатора при реакции полимеризации стирола.
Численные значения теплот образования комплексов титана, циркония и тория, полученные автором, подтвердили, что связь между металлом и кислородом адденда донорно-акцепторная. Это позволило установить диссоциацию некоторых комплексных соединений и показать, что она может протекать ступенчато.
Разработан новый метод расчета теплот смешения для систем с химическим взаимодействием. Он имеет то преимущество перед другими, что дает возможность точно установить состав соединений даже в иррациональных системах. Показано, что изменение полярности комплексных соединений галогенидов с органическими аддендами в ряду хлорид-бромид-йодид металла зависит от положения металла в периодической системе.
Найдя в первом приближении величину внутреннего локального поля и на основании этого - величину функции Ланжевена, О. А. Осипов дает теоретическое истолкование эмпирической формуле Я. К. Сыркина.
О. А. Осипов вывел формулу, устанавливающую связь между диэлектрической проницаемостью чистой полярной жидкости и ее дипольным моментом. Пользуясь ею, можно не только с большой точностью определить дипольный момент чистой полярной жидкости, но и дипольный момент полярного вещества в полярном растворителе, что имеет практический интерес, так как многие вещества в неполярных растворителях не растворяются, ввиду чего формула Дебая к ним неприменима. Выведено уравнение для определения степени диссоциации и константы нестойкости токнепроводящих комплексных соединений. Найдено уравнение, связывающее поверхностное натяжение с дипольным моментом. Введено понятие об условном дипольном моменте как величине, определяющей полное межмолекулярное взаимодействие.
Кратко рассмотренные здесь результаты исследований О. А. Осипов обобщил в статьях (около 60). Важнейшие из них написаны им лично и в соавторстве.1
1 (О. А. Осипов. Доклады АН СССР, 102, 1171 (1955); ЖОХ, 26, 322 (1956); О. А. Осипов и И. К. Шеломов. ЖФХ, 30, 608 (1956); О. А. Осипов. ЖФХ, 31, 1543 (1957); О. А. Осипов и Ю. Б. Клетеник. ЖНХ, 4, 1494 (1959).)
О. А. Осипов не только сам успешно расширил и углубил исследования по физико-химическому анализу жидких систем, включив как компоненты соли редких металлов и применив разные физико-химические методы, но и привлек к этому способную молодежь. Так, изучение взаимодействия четыреххлористого титана со сложными эфирами одноосновных кислот успешно провел Ю. А. Лысенко. Он изучил взаимодействие четыреххлористого титана с тридцатью сложными эфирами одноосновных кислот и показал, в частности, что хлорид титана образует три эфирата: 2TiCl4×Э, TiCl4×Э, TiCl4×2Э.
По теплотам смещения и измерению дипольных моментов соединений состава 1:1, характерных для титана, установлено, что эфираты состава 1:1 и 1:2 получаются за счет до-норно-акцепторного взаимодействия, т. е. являются типичными молекулярными соединениями. Электролиз эфиратов указанного состава позволил представить схему их электролитической диссоциации.
Особенно интересным в теоретическом и практическом отношении является опытно установленный факт, что в эфиратах титана состава 1:1 органические адденды более активны, чем в соединениях состава 1:2. Это определяет характер их разложения, в результате которого получаются галоидные ал килы. Здесь проявляется полное сходство эфиратов титана с эфиратами хлористого алюминия. Ю. А. Лысенко высказал предположение о строении эфиратов титана и координационной емкости эфирных аддендов.
Результаты исследования были оформлены в кандидатскую диссертацию1, которую Ю. А. Лысенко успешно защитил на химическом факультете университета в 1959 г.
1 (Ю. А. Лысенко. Исследование взаимодействия четыреххлористого титана со сложными эфирами одноосновных кислот. Диссертация на соискание ученой степени кандидата химических наук. Ростов-на-Дону, 1959.)
Ю. Б. Клетеник работал в этом же направлении и результаты представил как кандидатскую диссертацию1, защищенную в Новочеркасском политехническом институте в 1959 г. Он изучил полярность 26 комплексных соединений галогенидов циркония со сложными эфирами одноосновных органических кислот. Эти комплексы характеризуются большими значениями дипольных моментов. По мере усложнения молекул одноосновых органических кислот, образующих эти эфиры, полярность и устойчивость комплексных соединений состава 1:2 закономерно уменьшается. На наш взгляд, ценным в этой работе является то, что автор не ограничивался констатированием фактов образования соединений, а методами препаративной химии индивидуализировал 8 молекулярных соединений галогенидов циркония со сложными эфирами состава 1:1.
1 (Ю. Б. Клетеник. Физико-химическое исследование некоторых молекулярных соединений галогенидов циркония и титана. Диссертация на соискание ученой степени кандидата химических наук. Ростов-на-Дону, 1959.)
Ю. Б. Клетеник, изучив величины дипольных моментов комплексных соединений галогенидов циркония и титана со сложными эфирами состава 1:2, установил, что они имеют цис-форму. Экспериментально обосновано, что комплексные соединения хлорида циркония состава 1:1 и 1:2 почти одинаково термически устойчивы и что по мере увеличения кислотности карбоновой кислоты термическая устойчивость эфиратов циркония закономерно уменьшается.
Заслуживает внимания тот факт, что четыреххлористый цирконий и четыреххлористый титан, а также образуемые ими комплексы с бензилацетатом способствуют поликонденсации хлористого бензила с образованием смол, которые могут иметь практическое значение.
При научном руководстве О. А. Осипова выполнена диссертация И. К. Шеломювым1, которая была защищена на степень кандидата химических наук в Новочеркасском политехническом институте в 1960 г. И. К. Шеломов изучил электрические свойства 19 двойных жидких систем, что позволило сделать ряд интересных выводов. Отметим некоторые из них.
1 (И. К. Шеломов. Некоторые вопросы физико-химии диэлектриков. Диссертация на соискание ученой степени кандидата химических наук. Ростов-на-Дону, 1960.)
Диссертант показал, что величина электростатического поля полярных жидкостей прямо пропорциональна дипольному моменту их молекул. Он экспериментально обосновал, что в случаях отсутствия химического взаимодействия между компонентами системы правило аддитивности поляризаций соблюдается при любых соотношениях данной пары компонентов, и теоретически доказал известное положение, согласно которому между диполыными моментами и диэлектрической проницаемостью полярных жидкостей существует тесная взаимосвязь. Им предложен метод нахождения константы нестойкости и вычисления степени диссоциации, исходя из молекулярных поляризаций. Пользуясь этим методом, определены константы нестойкости комплексных соединений в системах хлороформ- метил ацетат и хлороформ - диэтиловый эфир.
И. К. Шеломов получил уравнения, связывающие молекулярные объемы гетерополярных соединений с поверхностным натяжением, дипольный момент молекул с поверхностным натяжением и др.
Упомянем, что в этой же области физико-химического анализа работает М. А. Панина, а И. А. Решетниковым выполнено исследование, которое было оформлено в кандидатскую диссертацию, защищенную в университете в 1959 г.
Раскрывая кратко содержание работ по физико-химическому анализу жидких систем с применением электрических и магнитных методов исследования, мы нарушили хронологическую последовательность изложения. Поэтому возвращаем внимание читателей к научным работам, завершенным как кандидатские диссертации на кафедре физической химии под руководством Н. А. Трифонова.
Здесь прежде всего заслуживают упоминания работы Б. Я. Тейтельбаума. Диссертация его была посвящена рассмотрению поверхностного слоя двойных жидких систем с точки зрения их состава и строения. Он изучил уравнения изотерм поверхностного натяжения нормальных систем, которыми пользовались в разное время для этих целей, и указал условия и пределы их применимости. В результате он вывел уравнение и сделал интересное заключение о том, что максимум адсорбции в жидких двойных системах соответствует точке на изотерме поверхностного натяжения, подчиняющейся соотношению, в котором поверхностное натяжение системы равно корню квадратному из произведения величин поверхностного натяжения компонентов системы.
Б. Я. Тейтельбаум разработал объективный автоматический способ фоторегистрации показаний манометра и сконструировал удобный манограф. Применение их исключает ошибки, возможные при визуальном способе отсчета, что убедительно подтверждено опытными данными. Им экспериментально было изучено по вязкости, плотности, показателю преломления и поверхностному натяжению восемь двойных жидких систем. Изотермы вязкости и особенно плотности и показателей преломления свидетельствуют об отсутствии химического взаимодействия между компонентами изученных систем.
Интересное явление он наблюдал при изучении системы мезитилен - метиловый спирт. Компоненты этой системы при взбалтывании дают устойчивую пену. Б. Я. Тейтельбауму удалось снять изотермы стойкости пены и показать, что она увеличивается с понижением температуры; максимальная же стойкость ее отвечает примерно эквивалентному соотношению мезитилена и метилового спирта. Прибавление к пенообразующим компонентам системы небольших количеств воды повышает стойкость пены.
Явление пенообразования следовало бы проанализировать и увязать с известным бичом паросилового и паровозного хозяйства - вспениванием и выбросом котловых вод. Этому вопросу много .работ посвятили С. А. Дуров и В. Г. Глейм.
Касаясь состава поверхностного слоя и строения жидкостей, Б. Я. Тейтельбаум подчеркивает необходимость его совместного решения. Так, в системах бензол - этиловый эфир и мезитилен - этиловый эфир он рассчитал и состав поверхностного слоя, и геометрические константы в нем.
Степень кандидата химических наук Б. Я. Тейтельбаум получил, защитив диссертацию1 на химфаке университета в 1947 г. В настоящее время он успешно ведет научную работу в Казанском филиале АН СССР.
1 (Б. Я. Тейтельбаум. Состав и строение поверхностного слоя двойных жидких систем. Диссертация на соискание ученой степени кандидата химических наук. Ростов-на-Дону, 1947.)
К этому же времени относится работа Н. П. Мельниковой, выполненная под руководством Н. А. Трифонова и М. С. Острикова. По своему направлению она примыкает к школе академика П. А. Ребиндера.
Применив метод затухающих колебаний, Н. П. Мельникова впервые установила случаи повышения твердости кварцита под растворами соды и мыла, а также мрамора под растворами щавелевой кислоты, щавелевокислого аммония, фосфата аммония, хлорида бария и нитратов натрия и стронция. Повышение твердости мрамора под указанными растворами подтверждено методом шлифования. ""Повысители твердости" (в данном случае растворы всех поименованных веществ) образуют на поверхности тела, в зоне предразрушения, цементирующее соединение. Чтобы проверить склерометрические данные и выяснить механизм повышения твердости, Н. П. Мельниковой изучено действие указанных реагентов на поверхностях раздела методом седиментационных объемов.
Н. П. Мельникова показала, что между изменениями твердости и величин седиментационных объемов (в изученных ею случаях) есть прямая зависимость как при понижении твердости, так и при ее повышении. При изучении влияния склероагентов на прочность стеклянных пластинок установлено, что свойство твердого тела в зависимости от изменения молекулярной природы среды может уменьшаться и увеличиваться.
"Явление повышения твердости - не исключение, а вполне закономерный результат определенных физико-химических поверхностных процессов,- пишет Н. П. Мельникова.- Явление повышения твердости - вторая сторона общего учения о физико-химическом изменении твердости".1
1 (Н. П. Мельникова. Исследование физико-химического повышения твердости. Диссертация на соискание ученой степени кандидата химических наук. Ростов-на-Дону, 1948, стр. 172.)
Один и тот же склероагент может проявлять себя и как понизитель, и как повыситель твердости в зависимости от его концентрации. Результаты исследований Н. П. Мельникова представила как кандидатскую диссертацию, которую защитила на химфаке университета в 1948 г.
Изучением поверхностного натяжения двойных систем, содержащих ассоциированные жидкости, занималась К. Н. Коваленко.
Ею исследовано 20 систем, главным образом по поверхностному натяжению и частично по вязкости, плотности и показателю преломления. При этом показано, что выпуклость изотерм поверхностного натяжения двойных жидких систем, компоненты которых представляют собой химически невзаимодействующие, но ассоциированные жидкости, может быть объяснена различной степенью ассоциации исходных веществ, сжатием системы при смешении компонентов, взаимодействием их диполей и различием в размерах молекул.
Установлено, что низшие спирты гомологического ряда в бездипольных растворителях (в бензоле, нафталине, дифенил-метане) ведут себя, как аномальные активные вещества. Этим обусловлен тот факт, что они дают изотермы адсорбции и поверхностного натяжения с областью перегиба, которая соответствует слабым растворам спирта в растворителе.
По утверждению К. Н. Коваленко, "кривые полной поверхностной энергии, вычисленной по уравнению Гиббса-Гельмгольца для систем, содержащих поверхностно-активное вещество, по форме подобны кривым температурного коэффициента поверхностного натяжения и являются достаточно характерными. Они резко изменяются с температурой, отражая падение поверхностной активности"1.
1 (К. Н. Коваленко. Поверхностное натяжение двойных систем, содержащих ассоциированные жидкости. Диссертация на соискание ученой степени кандидата химических наук, Ростов-на-Дону, 1947, стр. 18-б.)
Далее отмечается, что изучение жидких систем при температуре инверсии интересно при измерении поверхностного натяжения, так как позволяет подмечать слабое химическое взаимодействие между компонентами системы и даже распад компонентов при их взаимном растворении. Указанное положение подтверждено опытно в системах: аллиловое горчичное масло - этилаяилин; изоамиловый спирт - этилацетат; пиридин - этилаяилин.
По форме изотерм поверхностного натяжения К. Н. Коваленко установила в системах хинолин - этиланилин, пиридин - этиланилищ хинолин - анилин химические соединения, которые затем были подтверждены измерением других свойств: показателя преломления, плотности и в особенности вязкости, отразившей эти соединения на кривых как типичные для иррациональных систем.
В работе показано, что кривые температурного коэффициента поверхностного натяжения нехарактерны, т. е. не согласуются с данными изотерм. Такое несоответствие объясняется "большой ошибкой в определении этой величины"1.
1 (К. Н. Коваленко. Поверхностное натяжение двойных систем, содержащих ассоциированные жидкости. Диссертация на соискание ученой степени кандидата химических наук, Ростов-на-Дону, 1947, стр. 18-б.)
Кандидатскую диссертацию, выполненную под руководством Н. А. Трифонова, К. Н. Коваленко защитила на химфаке университета в 1948 г.
В дальнейшем К. Н. Коваленко углубила исследование по жидким системам, занявшись изучением электрических свойств компонентов. Результаты систематически освещаются в периодической печати. Ею опубликовано по вопросам физико-химического анализа 22 статьи.
Теоретической обработкой опытных материалов наряду с экспериментальными исследованиями успешно занимался Н. Л. Ярым-Агаев. В частности, он дал удачную термодинамическую трактовку физико-химическому повышению твердости. Анализируя литературные данные по твердости (П. А. Ребиндер, В. Д. Кузнецов, Е. Е. Горбовский), выводы из экспериментальных материалов Н. П. Мельниковой и пользуясь классическим уравнением Гиббса, Н. Л. Ярым-Агаев предложил термодинамическое обоснование зависимости поверхностной твердости тела от концентрации раствора, под которым оно находится. Эта зависимость выражена математической формулой, дающей возможность предусматривать случаи, когда твердость падает, остается без изменения или увеличивается1. Ряд интересных работ, выполненных на кафедре физической химии, он опубликовал в различных периодических изданиях2.
1 (Н. Л. Ярым-Агаев. Сообщение о научных работах членов ВХО им. Д. И. Менделеева, вып. 1, 1947, стр. 26.)
2 (Н. Л. Ярым-Агаев.. ЖНХ, 1, вып. 3 (1956); ЖФХ, 24, 1061 (1950); Изв. сектора ФХА, 20, 361 (1950).)
Диссертация на соискание ученой степени кандидата химических наук им успешно защищена в ИОНХе АН СССР в 1948 г.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'