
Демонстрация химических опытов при повторении
Демонстрации предметов, процессов и изобразительных средств наглядности могут применяться: при повторении непосредственно за изучением нового учебного материала и на последующих занятиях перед изучением нового учебного материала, а также при обобщающем повторении после изучения какой-либо темы или части курса. Рассмотрим некоторые общие приемы демонстрации опытов при повторении на примере процесса усовершенствования знаний о свойствах галогенов. При изучении химических свойств галогенов обращается внимание па взаимодействие свободных элементов с металлами и водородом. Чтобы показать химическую активность этих элементов в отношении к металлам, демонстрируют очень эффектные опыты: горение в атмосфере хлора различных металлов. Не устояв против соблазна вызвать интерес учащихся внешними признаками явлений, учитель часто излишествует в демонстрациях опытов: показывает горение разных металлов только потому, что наблюдается яркое, занимательное явление, хотя химические реакции во всех случаях сходны и для выражения их сущности пишут сходные уравнения реакции.
Педагогический эффект от такого излишества получается противоположный тому, который ожидал учитель: первые опыты учащиеся наблюдают с интересом, активно участвуют в разборе их на основе атомно-молекулярного учения, а последние опыты только наблюдают уже при пониженном внимании. Это можно объяснить тем, что после разбора первых опытов и написания уравнений химических реакций последующие опыты и их анализ не представляют уже значительного интереса.
"Закрепление" же знаний в конце урока или на следующем занятии в большинстве случаев проводится без использования средств наглядности, при пониженном интересе учащихся, что приводит к неудовлетворительным результатам. А между тем имеется возможность активизировать деятельность учащихся, а для этого в конце урока можно показать некоторые опыты при повторении изученного на уроке. Например, если в начале урока учитель показал опыт горения натрия в атмосфере хлора, провел его анализ и сделал первый вывод о взаимодействии хлора с металлами, то горение железа в хлоре следует показать в конце урока или на следующем уроке. При демонстрации этого опыта учитель напоминает учащимся о сходстве натрия и железа в их отношении к кислороду. Затем предлагает рассказать учащимся о том, как происходило горение натрия в хлоре, посмотреть, как реагирует железо с хлором. При анализе этого опыта обращается внимание не только на тепловой эффект реакции (что является общим с реакцией соединения натрия с хлором), но и на состав продукта взаимодействия железа с хлором (на состав хлорного железа). Важно отметить, что железо в хлорном железе трехвалентно. Это указывает на большую химическую активность хлора в отношении к железу.
Описанная форма сочетания слова учителя с показом опыта сходна со второй формой, применяемой при изучении нового учебного материала, но отличается более резко выраженным сходством и экспериментальными задачами. Демонстрации опытов, характеризующих химическую активность хлора, можно включать в вводную беседу на уроке при изучении хлористого водорода, при повторении свойств хлора. В этой повторной демонстрации обращается внимание учащихся не столько на тепловой эффект, сколько на продукт этой реакции, который подлежит изучению на предстоящем уроке.
При этом возможны две формы сочетания слова учителя со средствами наглядности:
1. Учитель рассказывает учащимся об опыте, который они раньше наблюдали, и о тех выводах, которые были сделаны тогда на основе этого опыта, а затем демонстрирует опыт, обращая внимание на образование "дымящегося" газа.
2. В вводной беседе учитель предлагает учащимся вспомнить о взаимодействии хлора с водородом, как о свойстве хлора и рассказать об опыте, который они наблюдали, выясняет, заметили ли они образование газа. После этого ставить вопрос: какое вещество получается в результате этой реакции?
Первая подготовка учащихся к наблюдению опыта напоминает третью форму сочетания слова со средствами наглядности, а второй способ подготовки к опыту - вторую форму. Отличие же их состоит в том, что обе они направлены на то, чтобы побуждать учащихся на активизацию деятельности памяти.
Применяется при повторении и третий способ повторения демонстрации, который можно назвать условно способом неполного повторения демонстрации. Например, после изучения основных и кислотных окислов учитель наметил такое повторение пройденного, при котором особенно резко выделяются характерные химические свойства окислов; их отношение к кислотам и к щелочам. Чтобы напомнить учащимся о взаимодействии основных окислов с кислотами, учитель демонстрирует не весь опыт, а показывает лишь какой-либо основной окисел, кислоту и соль. От учащихся требуется восстановить в памяти весь опыт, рассказать о нем и написать уравнение реакции.
Значительное оживление в классе вызывает также простое оформление опыта. На демонстрационный столик учитель ставит стеклянную банку с этикеткой СuО (формула написана крупными буквами), а на учительском столе ниже этой банки ставит склянку с соляной кислотой, на этикетке которой написана крупными буквами формула кислоты, а немного правее, на небольшой подставке, находится банка с хлорной медью и склянка с раствором этой же соли. Учащиеся рассказывают об этом опыте (рис. 11). Таким же приемом учитель может воспользоваться и для повторения опыта взаимодействия двуокиси углерода с едким кальцием. В этом случае средства наглядности приобретают главное значение, слово учителя ограничивается пояснением того, что написано на этикетках демонстрируемых склянок, и формулированием основного вопроса. Повторные демонстрации опытов применяются при обобщающем повторении после изучения какого-либо раздела курса или темы. Например, при сравнении свойств галогенов в конце изучения темы учитель обычно показывает образцы хлора, брома, йода с целью сравнения их физических свойств. При этом или сам сопоставляет физическое состояние этих веществ с величинами их атомных масс и других констант, или же проводит беседу, в которой учащиеся должны на основе повторных наблюдений сделать выводы о том, что галогены, имеющие большую атомную массу, имеют более высокую температуру плавления.
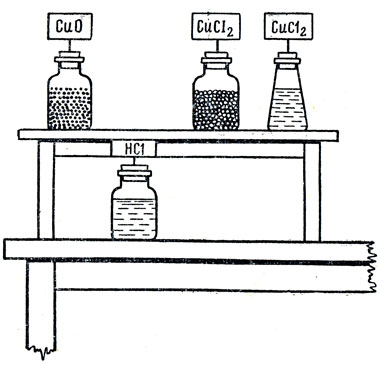
Рис. 10. Расположение реактивов на демонстрационном столе
При повторении можно демонстрировать такие опыты, которые сходны в каком-либо отношении с показанными ранее, но не являются их копиями. К атому железа присоединяется такое количество атомов хлора, которое соответствует высшей степени окисления этого элемента. Таким образом, учащиеся узнают общее и особенное во взаимодействии с хлором двух металлов, что важно для правильной характеристики не только металлов, но и хлора. Обобщив имеющиеся сведения, можно рассмотреть взаимодействие хлора и с другими металлами, не производя химических - опытов. Так же можно знакомить учащихся с взаимодействиями хлора с водородсодержащими веществами.
При демонстрации этих опытов могут применяться различные формы сочетания слова учителя со средствами наглядности. Эти формы имеют черты сходства с теми, которые применяются при демонстрации опытов и наглядных пособий в процессе приобретения учащимися новых для них знаний, но вместе с тем существует и различие между этими формами. Чтобы усовершенствовать знания учащихся, учитель предлагает воспроизвести реакции соединения натрия с хлором, а затем ставит вопрос: может ли реагировать хлор с другими металлами, например с железом? После теоретических предложений на этот счет он демонстрирует опыт и предлагает учащимся объяснить его на основе атомно-молекулярной или электронной теории.
Повторение желательно дополнять новыми знаниями. В данном случае важно обратить внимание на то, что продуктом реакции является хлорид железа, в котором проявляется повышенная степень окисляемости этого элемента, что свидетельствует о большой химической активности хлора в отношении к железу.
Одну и ту же химическую реакцию молено демонстрировать в разных приборах. Горение водорода в атмосфере хлора нужно показать в приборе, в котором можно хорошо наблюдать пламя, а также и собирать хлористый водород. Можно показать один и тот же тип реакции, меняя реагирующие вещества.
Основная цель демонстрации опытов при повторении - закрепление знаний, их уточнение. Опыты демонстрируются и с целью развития умений учащихся применять эти знания.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'