
Воздух
Так как учащиеся ко времени изучения химии располагают значительными сведениями о свойствах и составе воздуха, то и в данном случае целесообразно вести изучение воздуха в форме повторения на базе атомно-молекулярной теории и вводить необходимые дополнения.
Урок можно начать с сообщения о том, что воздух изучен позже других веществ, значение которых для жизни человека несравненно меньше, чем значение воздуха. Объяснить это можно тем, что воздух прозрачен, не имеет запаха и вкуса. Изучение воздуха пошло успешно после того, как научились разделять газы. Здесь уместно отметить работы М. В. Ломоносова и его высказывания об участии воздуха в процессе прокаливания металлов. После такого предисловия следует предоставить слово учащимся для сообщения о том, что они знают о составе воздуха, а потом предложить им продумать способ практического определения состава воздуха: какая часть воздуха приходится на долю кислорода, азота, углекислого газа.
Учащиеся обычно описывают опыт горения свечи под колпаком, погруженным открытой стороной в воду. Учитель, одобрив этот опыт, указывает и на его недостаток. В результате горения свечи образуются газообразные вещества, которые примешиваются к оставшейся части газа и затрудняют точно определить, сколько кислорода израсходовано на горение свечи. Чтобы точнее определить, какая часть воздуха по объему приходится на долю кислорода, нужно произвести сжигание в воздухе в закрытом сосуде такого вещества, окисел которого - твердое вещество. Таким веществом является фосфор, окисел его при обыкновенной температуре хорошо растворим в воде. Опыт можно провести в приборе, изображенном на рисунке 33.
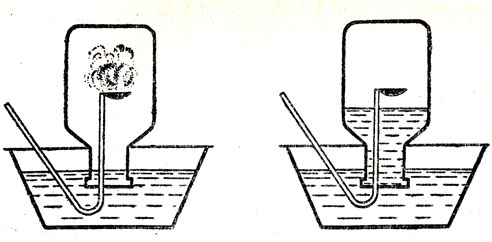
Рис. 33. Прибор для приближенного определения объема кислорода в данном объеме воздуха
К распространенным ошибкам учащихся относятся их сообщения, что углекислый газ составляет 3% от всего объема воздуха. Чтобы дать наглядное и правильное представление о незначительном количестве углекислого газа в воздухе, можно показать такой опыт: в две пробирки налить известковой воды и пропускать в одну из них воздух из газометра, а в другую углекислый газ до появления мути в пробирке. Учащиеся увидят, что от первого же пузырька чистого углекислого газа в пробирке с известковой водой появляется муть. Можно получить тоже самое и в другой пробирке, для этого необходимо пропустить через известковую воду около 3 л воздуха. После этого учащиеся лучше представят себе, что значит в воздухе содержится около 0,03% углекислого газа.
Ввиду того что инертные газы широко используются в различных отраслях производства "и особенно в светотехнике, нельзя умалчивать о них при изучении состава воздуха. По крайней мере нужно сообщить об аргоне и неоне. Из других инертных газов можно назвать гелий, как очень легкий газ, имеющий применение в воздухоплавании.
Затем следует обратить внимание учащихся на нахождение в воздухе пыли, влаги, микроорганизмов.
При ознакомлении с составом воздуха, естественно, возникает вопрос: является ли воздух механической смесью газов или их химическим соединением? Чтобы получить правильный ответ на этот вопрос, следует обратить внимание учеников на то, что свойства кислорода, азота и углекислого газа сохраняются в воздухе так же, как свойства железа и серы сохраняются в их смеси. Кроме того, при смешении кислорода, азота и углекислого газа не происходит ни выделения, ни поглощения теплоты или какого-либо иного вида энергии. По этим признакам учащиеся могут сделать правильный вывод о том, что воздух - смесь газов. Демонстрация жидкого воздуха убеждает учащихся в том, что воздух не имеет определенной точки кипения и разгоняется, как смесь жидких веществ.
Большое впечатление на учащихся производит опыт с жидким воздухом, так как они получают при этом яркие представления о низких температурах, при которых замерзает ртуть, изменяются свойства каучука и других веществ. Можно также показать изменение скорости реакции в зависимости от концентрации на примере горения ваты, смоченной жидким кислородом. За неимением жидкого воздуха полезно показать соответствующие диапозитивы и рассказать о свойствах жидкого воздуха. О нахождении и роли воздуха в природе учащиеся могут получить сведения из учебника. Самостоятельную работу можно организовать по приведенному ниже заданию.
Воздух в природе и использование его в промышленности
1. Прочитайте еще раз в учебнике химии § 26 о составе воздуха и кратко напишите, какие газы, входящие в состав воздуха, используются растениями и животными для их жизни.
2. Зная, что воздух - смесь газов, укажите, как можно получить из воздуха чистый азот и чистый кислород,
3. Почему после грозы воздух кажется особенно свежим?
В обобщающей беседе учитель исправляет неточности в отчетах учащихся, вносит дополнения и останавливается на получении кислорода способом сжижения и разгонки жидкого воздуха.
|
ПОИСК:
|
© CHEMLIB.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://chemlib.ru/ 'Библиотека по химии'